



Les piles
(Utilisation d'une réaction chimique pour obtenir de l'énergie électrique )
|
|
|
|
|
|
Ce qui suit est un document libre créé, en grande partie, par le groupe Sciences Physiques de l'Académie de Toulouse
En 1786, Galvani professeur d'anatomie à Bologne découvre par hasard que des cuisses de grenouilles suspendues par un crochet de cuivre à un balcon de fer subissaient des contractions violentes lorsqu'elles venaient en contact avec le fer; il émet l'hypothèse d'un fluide animal qui s'écoule par les métaux.
Mettant en doute cette théorie, Volta entreprend des recherches et établit en 1793 sa "série des tensions pour les métaux". En 1800, il découvre la pile électrique qui portera son nom.
I. Notion díoxydoréduction.
1. Un métal peut-il réagir avec un ion métallique ?
Observations 1 :
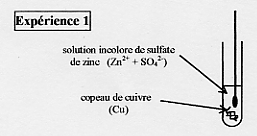
Il ne se passe rien. La température ne varie pas et il níy a aucune réaction entre le cuivre ( Cu ) et les ions zinc ( Zn2+ ).
Observations 2 :
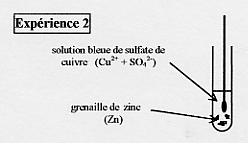
- la température du milieu réactionnel s'élève.
- le zinc se recouvre díun dépôt orangé : cíest du cuivre ( Cu ).
- la couleur bleue de la solution síatténue : la quantité díions cuivre ( Cu2+ ) diminue.
Il y a réaction entre le zinc ( Zn ) et les ions cuivre ( Cu2+ ).
La réaction entre un métal et l'ion d'un autre métal est donc possible ...mais dans certains cas seulement.
2. Comment interpréter cette réaction ?
Un atome du métal Zn se transforme en ion Zn2+ en libérant deux électrons.
Un ion Cu2+ de la solution capte ces deux électrons et se transforme en atome du métal Cu.
Au bilan, il y a échange díélectrons entre le métal zinc et les ions cuivre II.
|
|
traduit l'oxydation du zinc.
|
|
traduit la réduction des ions cuivre.
Au total,
|
|
est une réaction d'oxydoréduction.
Les électrons ne figurent pas dans le bilan global car ils sont simplement échangés.
Cette réaction spontanée libère de l'énergie sous forme de chaleur.
Plus généralement...
 Une réaction au cours de laquelle deux espèces chimiques échangent des électrons
est appelée réaction díoxydoréduction.
Une réaction au cours de laquelle deux espèces chimiques échangent des électrons
est appelée réaction díoxydoréduction.
 Líespèce chimique qui cède des électrons (donc qui s'oxyde) est un réducteur.
Exemple : Cu , Zn , ainsi que tous les métaux sont des réducteurs.
Líespèce chimique qui cède des électrons (donc qui s'oxyde) est un réducteur.
Exemple : Cu , Zn , ainsi que tous les métaux sont des réducteurs.
 Líespèce chimique qui capte des électrons (donc qui est réduite) est un
oxydant.
Líespèce chimique qui capte des électrons (donc qui est réduite) est un
oxydant.
Exemple : Cu2+, Zn2+, ainsi que tous les ions métalliques sont des oxydants.
 A tout oxydant on peut associer un réducteur; l'ensemble forme un couple
oxydant/réducteur.
A tout oxydant on peut associer un réducteur; l'ensemble forme un couple
oxydant/réducteur.
Exemple : Cu2+/Cu et Zn2+/Zn sont deux couples oxydant/réducteur.
3. Peut-on prévoir la réaction spontanée entre deux couples oxydant/réducteur ?
Les travaux de Volta ont permis d'associer un potentiel normal díoxydoréduction E0 (en V) à chaque couple oxydant/réducteur. A partir de ces valeurs, un classement de tous les couples a donc été possible.
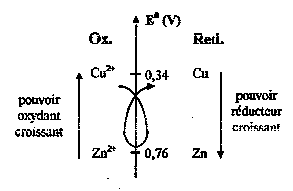
Plus E0 est grand, plus líoxydant du couple est fort et plus le réducteur est faible.
Exemple : Cu2+ est plus oxydant que Zn2+ et Zn est plus réducteur que Cu.
La réaction díoxydoréduction spontanée entre deux couples síeffectue toujours entre le réducteur le plus fort et líoxydant le plus fort (règle dite "du gamma").
Exemple :
|
|
Exercice.
a) En vous aidant de la table de classement des couples oxydant/réducteur, indiquer si une réaction est possible entre :
|
|
|
|
|
|
b) Si oui, écrire les équations bilans correspondantes ( n'écrivez pas sur l'écran...)
|
.......................................................................................... .......................................................................................... .......................................................................................... .......................................................................................... .......................................................................................... |
|
II. Quel est le principe díune pile ?
Une réaction díoxydoréduction naturelle transforme de l'énergie chimique en chaleur. La pile est un dispositif qui permet de transformer l'énergie chimique en énergie électrique.
1. La pile de Volta (cf. document).
La première pile est due au physicien italien A.Volta. En empilant dans cet ordre, un disque díargent, un disque de zinc, un disque en carton imbibé díeau salée ...et ainsi de suite , il síaperçut que la pile ainsi réalisée permettait díobtenir un courant électrique continu.
2. La pile Daniell.
a) Comment est-elle constituée ?

Le voltmètre branché aux bornes du dispositif indique la tension (ou différence de potentiel) :
UCu,Zn = VCu - VZn = 1,1 V
Ce dispositif est bien un générateur de courant électrique continu.
VCu - VZn > 0 d'où VCu > VZn
- la lame de Cu constitue la borne positive de la pile;
- la lame de Zn constitue la borne négative de la pile.
b) Quel est son fonctionnement ?
Le courant circule conventionnellement de la borne positive vers la borne négative dans le circuit extérieur à la pile; les électrons, qui se déplacent dans le sens opposé, quittent donc líélectrode de zinc pour arriver sur líélectrode de cuivre.
Quelle est l'origine du mouvement des électrons ?
Une pesée des électrodes montre que lorsque la pile débite, la masse de la lame de zinc diminue tandis que celle de la lame de cuivre augmente. Il faut donc admettre le principe suivant :
 A líélectrode négative du zinc passe en solution, transformé en ions Zn2+
selon líéquation :
A líélectrode négative du zinc passe en solution, transformé en ions Zn2+
selon líéquation :
Zn (métal)  Zn2+(solution)
+ 2 e- Il
y a oxydation du zinc.
Zn2+(solution)
+ 2 e- Il
y a oxydation du zinc.
Les électrons libérés vont pouvoir quitter líélectrode et traverser le circuit extérieur.
 A líélectrode positive les ions Cu2+ de la solution se déposent à l'état
de cuivre selon líéquation :
A líélectrode positive les ions Cu2+ de la solution se déposent à l'état
de cuivre selon líéquation :
Cu2+(solution)
+ 2 e-  Cu (métal) Il
y a réduction des ions cuivre.
Cu (métal) Il
y a réduction des ions cuivre.
Les électrons nécessaires à cette réduction arrivent à líélectrode positive par le circuit extérieur, en provenance de la lame de zinc.
Au bilan, le fonctionnement de la pile Daniell est assuré par une réaction díoxydoréduction dans laquelle le métal Zn est oxydé en ions Zn2+ tandis que les ions Cu2+ sont réduits en métal Cu.
Zn + Cu2+
 Zn2+ + Cu Cette
réaction est spontanée.
Zn2+ + Cu Cette
réaction est spontanée.
... et quel est le rôle du pont salin ?
La solution de sulfate de zinc s'enrichit en ions Zn2+ au niveau de la borne négative.
La solution de sulfate de cuivre s'appauvrit en ions Cu2+ au niveau de la borne positive.
Pour rétablir la neutralité électrique de chaque solution il faut que les ions sulfate puissent migrer de la deuxième solution vers la première solution à travers le pont salin.
c) Comment caractériser cette pile ?
 par sa chaîne conductrice, symbolisée par :
par sa chaîne conductrice, symbolisée par :
pôle (-) couple de demi-pile « pont salin » couple de demi-pile pôle (+)
Exemple : Dans le cas de la pile Daniell la chaîne conductrice s'écrit :
(-) Zn / Zn2+ // Cu2+ / Cu (+)
 par sa force électromotrice (ou f.e.m.).
par sa force électromotrice (ou f.e.m.).
C'est la tension mesurée entre les bornes de la pile quand elle ne débite pas. On la note E ; elle síexprime en volt (V).
La f.e.m. d'une pile peut être calculée à partir des valeurs des potentiels d'oxydoréduction des deux couples constituant les demi-piles.
E = E0(1/2 pile de la borne +) - E0(1/2 pile de la borne -)
Exemple : La f.e.m. de la pile Daniell a pour valeur :
E = E0(+) - E0(-) = 0,34 - (-0,76) = 1,10 V ce que confirme l'expérience.
III. Les piles électrochimiques usuelles.
La pile réalisée précédemment présente certains inconvénients et n'est pas transportable.
- risque d'écoulement des solutions ioniques (ou électrolytes); pour y remédier on gélifie ces solutions et on parle alors de pile sèche.
- encombrement trop important de la pile qui ne délivre par ailleurs que des courants de trop faible intensité (une dizaine de mA au plus).
La chaîne conductrice a donc été modifiée,
(-) métal / électrolyte // oxydant + électrolyte / électrode inerte mais conductrice (+)
...mais le principe reste identique :
- à la borne - le métal perd des électrons et s'oxyde;
- à la borne + líoxydant gagne des électrons et se réduit.
1. Les piles salines type Leclanché (cf. document).
La chaîne électrolytique est la suivante.
(-) Zn amalgamé / NH4+ + Cl- acidifié // MnO2 et NH4++ Cl- / C graphite (+)
Líélectrolyte est une solution gélifiée de chlorure díammonium (NH4+ + Cl-). Ce composé ionique était appelé autrefois sel, díoù le nom de pile saline.
2. Les piles alcalines type Mallory (cf. document).
Le zinc et le carbone sont utilisés dans ce cas sous forme de poudre : ils sont donc plus réactifs.
Líélectrolyte est une solution gélifiée díhydroxyde de potassium (K+ + OH-). Le potassium (K) étant un métal alcalin, on parle ici de pile alcaline.
Ces piles sont plus chères que les précédentes mais plus performantes.
3. Les piles boutons (cf. document).
Le développement de dispositifs électroniques miniaturisés tels que les montres, les calculatrices, les appareils auditifs ... a conduit à mettre au point les piles boutons de très faible encombrement (1 cm de diamètre et quelques millimètres díépaisseur).
Ce sont des piles alcalines mais le dioxyde de manganèse est remplacé par díautres oxydants comme líoxyde de mercure (HgO) ou líoxyde díargent (Ag2O).
Attention : il ne faut pas jeter ce type de piles mais les collecter car le mercure est hautement toxique.
4. Une nouveauté : la pile au lithium.
Dans ce cas, le zinc est remplacé par le lithium. Or celui-ci comme tous les métaux alcalins réagit violemment avec líeau. Il faut donc remplacer líélectrolyte par des solutions organiques.
Ces contraintes expliquent le coût de ces piles, très supérieur à celui des piles classiques.
IV. Performances des piles.
En dehors de la f.e.m. E (définie précédemment), deux autres grandeurs permettent de comparer les différentes piles.
1. La capacité (ou charge).
C'est la quantité díélectricité totale que peut fournir la pile.
On la note Q; on l'exprime en coulombs (C).
Si la pile débite un courant d'intensité constante I pendant la durée t, la quantité d'électricité Q fournie est donnée par la relation :
|
|
I : intensité (en A) ; t : durée (en s) ; Q : quantité d'électricité (en C)
Remarque : Si I est exprimé en ampère et t en heure, alors Q síexprime ampère-heure (A.h).
1 h = 3600 s donc 1 A.h = 3600 C
2. Líénergie emmagasinée.
C'est l'énergie chimique totale susceptible d'être transformée en énergie électrique.
On la note W (pour éviter la confusion possible avec la f.e.m. E); on l'exprime en joules (J).
Si une pile de f.e.m. E constante, débite un courant díintensité I constante pendant la durée t, l'énergie électrique produite est donnée par la relation :
|
|
W = E.I.t = E.Q E : f.e.m. (en V) ; I : intensité (en A) ; t : durée (en s) ;
Q : quantité d'électricité (en C) ; W : énergie (en J).
Informations.
Dans la pratique, toutes les recherches tendent à obtenir des piles emmagasinant le plus díénergie possible pour une masse ou un volume le plus faible possible.
On a donc été amené à définir :
|
|
|
W en J ; m en kg ; Wm en J.kg-1 ; V en m3 ; WV en J.m-3
Exemples :
Compléter le tableau des données suivantes.
|
piles |
E (en V) |
Q en (A.h) |
W (en J) |
m (en g) |
Wm (en J/kg) |
V (en m3) |
Wv (en J/m3) |
|
|
Référence |
Type |
|||||||
|
LR03 |
alcaline |
1,50 |
1,05 |
|
11 |
|
3,8.10-6 |
|
|
MR8 |
mercure |
1,35 |
0,08 |
|
1,1 |
|
3,7.10-7 |
|
|
SR44 |
argent |
1,55 |
0,15 |
|
2,4 |
|
5,7.10-7 |
|
|
|