
Radioactivité
Découverte en 1896 par le français Henri Becquerel la radioactivité naturelle affecte le noyau des atomes.
Ecouter le son d'un compteur de Geiger
|
|
Plaque photo pourtant non insolée mais placée à proximité d'un sel d'uranium (26-27 février 1896).
A - Structure de l'atome:
|
|
|
|
|
Caractéristiques:
|
|
Protons |
Neutrons |
Electrons |
|
Symboles |
|
|
|
|
Masses |
|
|
|
|
Charges électriques |
|
|
|
Dans un noyau, le nombre de protons est noté Z. Ce nombre est appelé numéro atomique: C'est ce numéro qui permet de ranger l'atome dans la classification périodique des éléments.
Voir une classification périodique des éléments.
Dans un noyau, le nombre total de nucléons (c'est à dire le nombre de protons augmenté du nombre de neutrons) est noté A. Ce nombre est appelé nombre de masse. C'est, approximativement, la masse molaire de l'élément chimique correspondant, puisqu'on s'est arrangés, en choisissant le nombre d'Avogadro, pour qu'une mole de nucléons ait une masse de 1 gramme:

On représente un noyau par un symbole dans lequel X désigne l'élément chimique:
|
|
Dans un noyau, le nombre de neutrons, souvent noté N, s'obtient par différence:
|
|
Un élément chimique est l'ensemble des atomes de même Z.
Un nucléide est l'ensemble des atomes de même Z et de même A.
Sont qualifiés d'isotopes d'un élément chimique, l'ensemble des nucléides de même numéro atomique Z.
Tous les isotopes d'un élément chimique sont rangés dans la même case d'une classification périodique des éléments.
Exemples:
|
Remarques 1 |
|
deutérium, entre dans la composition de l'eau lourde D2O, ralentiss"euse" de neutrons |
tritium radioactif période 12,46 ans |
|
carbone14, radioactif
5 500 ans |
azote (Nitrogene) |
|
traceur non radioactif |
|
radioactif
7,1.108ans |
radioactif
4,5.109ans |
||
|
symbôle |
99,985% |
0.0156% |
0% |
99,89% |
1,11% |
traces |
|
99,759% |
0,0374% |
0,204% |
|
0,711% |
99,284% |
|
protons |
1 |
1 |
1 |
6 |
6 |
6 |
7 |
8 |
8 |
8 |
26 |
92 |
92 |
|
neutrons |
0 |
1 |
2 |
6 |
7 |
8 |
7 |
8 |
9 |
10 |
30 |
143 |
146 |
|
Remarques 2 |
3 isotopes de l'élément hydrogène, élément le plus répandu dans l'Univers |
3 isotopes de l'élément carbone |
|
3 isotopes de l'élément oxygène, élément le plus répandu dans la Terre. |
|
2 isotopes de l'élément uranium |
|||||||
Dans un atome, il y a le même nombre d'électrons et de protons. L'atome possède donc aussi Z électrons. L'atome est électriquement neutre. Si ce n'est pas le cas, ce n'est plus un atome mais un ion ( cation s'il y a un défaut d'électrons ---> charge globale positive, anion s'il y a un excès d'électrons ---> charge globale négative).
|
|
B - La radioactivité  :
:
Puisqu'elle affecte le nombre ou la nature des particules du noyau, la radioactivité naturelle agit sur A, Z ou sur ces 2 grandeurs.
Un noyau est dit radioactif  s'il émet un hélion ou noyau d'hélium 4. Il se transforme
en un noyau fils qui a 4 nucléons dont 2 protons de moins que le noyau
père.L'élément fils se trouve donc 2 cases avant l'élément
père dans la classification périodique des éléments.
s'il émet un hélion ou noyau d'hélium 4. Il se transforme
en un noyau fils qui a 4 nucléons dont 2 protons de moins que le noyau
père.L'élément fils se trouve donc 2 cases avant l'élément
père dans la classification périodique des éléments.
|
|
Hélion ou noyau d'hélium 4 (2 protons et 2 neutrons)
L'équation nucléaire générale est la suivante:
|
|
|
|
par exemple l'isotope 210 du polonium devient du plomb 206:
|
|
ou encore
|
|
Loi de conservation du nombre de nucléons: le nombre total de nucléons est le même à gauche et à droite de la flèche, soit, pour l'exemple suivant ( 238 = 234 + 4 )
Loi de conservation de la charge: (92 = 90 + 2 ) dans l'exemple suivant
|
|
Ce rayonnement est arrêté par 6 cm d'air ou par une feuille de papier.
C - La radioactivité  :
:
Un noyau est radioactif  s'il libère un électron ( charge -e, masse
s'il libère un électron ( charge -e, masse  0 ). Le symbole de l'électron est:
0 ). Le symbole de l'électron est:

L'équation générale est:
|
|
Même nombre A de nucléons ; un proton de plus, un neutron de moins.
La radioactivité  est la qualité des noyaux qui ont trop de neutrons par rapport
aux protons.
est la qualité des noyaux qui ont trop de neutrons par rapport
aux protons.
Le noyau fils a le même nombre de masse que le noyau père mais il se trouve une case plus loin dans la classification périodique des éléments.
L'électron ne vient pas du nuage électronique mais est créé par le noyau instable, ce qui s'accompagne d'une profonde modification de ce noyau.
Exemples:
|
|
|
|
Ce rayonnement est arrêté par une feuille d'aluminium.
D - La radioactivité 
Un noyau est radioactif  s'il cède un positron ou "électron positif" dont
le symbole est:
s'il cède un positron ou "électron positif" dont
le symbole est:

Equation générale:
|
|
Même nombre A de nucléons ; un proton de moins, un neutron de plus.
La radioactivité  est la qualité des noyaux qui n'ont pas assez de neutrons
par rapport aux protons.
est la qualité des noyaux qui n'ont pas assez de neutrons
par rapport aux protons.
Le noyau fils se trouve juste avant le noyau père dans la classification périodique des éléments.
Exemples:
|
|
|
|
Ce rayonnement est, lui aussi, arrêté par une feuille d'aluminium.
E - La radioactivité ou émission 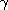
Au cours des 3 types précédents de radioactivité, le noyau fils peut se trouver
dans un état excité. Ce produit acquiert alors un état plus stable en se désexcitant
par émission d'un grain de lumière appelé photon noté 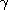 . Le photon n'a ni charge, ni masse. On peut le représenter par
. Le photon n'a ni charge, ni masse. On peut le représenter par

Equation générale:
|
|
Noyaux père et fils sont d'un même nucléide.
Ce rayonnement est très pénétrant; il peut traverser une épaisse plaque de plomb, un coffre-fort. Le béton l'arrête.
En résumé, les 4 types de radioactivité:
|
|
F - Loi de décroissance radioactive:
Soit N (t) la population de noyaux non désintégrés à un instant générique t.
|
On appelle activité et on la note |
|
le nombre de désintégrations par seconde. |
|
|
s'exprime en becquerels ( symbole Bq; 1 Bq = 1 désintégration par seconde ). Ancienne unité: 1 Curie = 3,7.1010 Bq (activité de 1 gramme de Radium 226). |
|
|
Elle est proportionnelle au nombre N de noyaux non encore désintégrés. |
|
|
On a donc:

|
|
Loi de décroissance radioactive.
|
|
La période ou temps de demi-vie est la durée au bout de laquelle la population a diminué de moitié:

|
|
Voici quelques exemples de périodes: